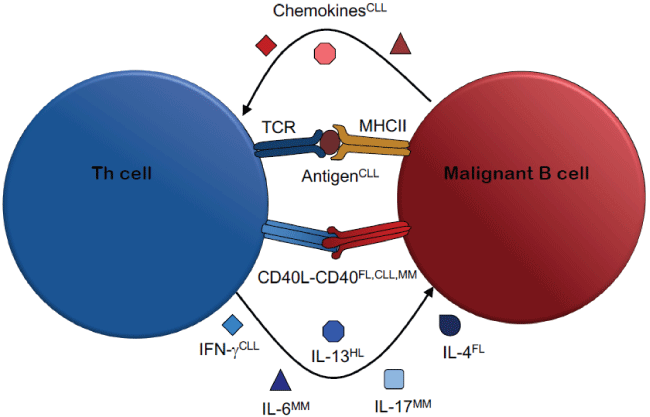
图1:恶性Th细胞- b细胞相互作用的机制

西蒙行窃*
实验传染病和癌症研究,苏黎世大学儿童医院,苏黎世,瑞士*通讯作者:Simone Burgler,实验传染病和癌症研究,苏黎世大学儿童医院,苏黎世,瑞士,电子邮件:simone.buergler@kispi.uzh.ch
辅助性T细胞和B细胞的协作对于产生具有不同效应功能的高亲和力抗体至关重要,从而建立有效的免疫应答。生理T细胞帮助B细胞发生在外周血淋巴器官的生发中心,滤泡T辅助细胞与成熟的、抗原刺激的B细胞相互作用。偶尔,B细胞发生恶性转化,可能导致白血病或淋巴瘤的发展。在几乎所有的癌症中,肿瘤细胞的生长和生存都严重依赖于与肿瘤微环境的相互作用。由于许多B细胞恶性肿瘤发生在生发中心——生理上T辅助细胞和B细胞相互作用的场所——T辅助细胞是B细胞白血病和淋巴瘤肿瘤微环境的主要组成部分。因此,虽然辅助T细胞和B细胞之间的相互作用对有效免疫反应的发展至关重要,但在另一方面,有助于B细胞恶性肿瘤的发展和发病。这篇小型综述讨论了辅助T细胞介导的支持恶性B细胞在白血病和淋巴瘤的机制。鉴于肿瘤微环境在肿瘤发病机制中的重要性,针对这些恶性相互作用可以提高治疗效率,减少疾病复发。
辅助性T细胞;B细胞;白血病;淋巴瘤;B细胞恶性肿瘤;辅助性T细胞-B细胞相互作用;肿瘤微环境
慢性淋巴细胞白血病:慢性淋巴细胞白血病;FL:滤泡性淋巴瘤;霍奇金淋巴瘤:霍奇金淋巴瘤;MHC:主要组织相容性复合体;毫米:多个淋巴瘤;细胞受体T细胞受体
抗体是适应性免疫系统的中枢。抗体具有高度多样性和不同的效应功能,通过不同的机制识别和中和入侵的病原体。虽然B细胞是抗体的制造者,但它们依赖于辅助T细胞的帮助,产生具有不同效应特性的高亲和力抗体。因此,特异性和高效的免疫应答的建立需要Th细胞和B细胞的密切合作。
Th细胞在骨髓(BM)中生成但在胸腺中成熟。幼稚的Th细胞离开胸腺并迁移到周围,在那里它们可能遇到抗原呈递细胞呈递的抗原肽。在刺激下,Th细胞增殖并分化为表型和功能不同的几种效应子亚群之一。其中最具特征的是Th细胞e表达干扰素(IFN)-γ的促炎性Th1细胞和产生白细胞介素(IL)-4、IL-5和IL-13的Th2细胞[1]。除了Th17、Th9或Th22等其他效应细胞系外,还存在若干具有调节或抑制功能的Th细胞亚群,称为调节性T(Treg)细胞[2]。此外,还存在滤泡辅助性T(Tfh)细胞构成了一个独特的Th细胞群体,与滤泡外和外周Th细胞不同[3]。
B细胞在骨髓中发育成熟,随后迁移到次级淋巴器官,进入抗原依赖阶段。虽然这一过程可以独立于T细胞的帮助,但B细胞通常参与T细胞依赖的反应,并接受来自Tfh细胞[4]的CD40L、IL-4和IL-21的刺激。B细胞进一步发展成短命的浆细胞或GC B细胞,GC B细胞产生长寿命的记忆B细胞和浆细胞。重要的是,与Tfh细胞的相互作用导致激活诱导胞苷脱氨酶(AID)的上调,这是一种dna编辑酶,引发体细胞高突变(SHM)和类开关重组(CSR),这是创建具有多种效应功能的高亲和力抗体[5]的基本机制。
在其发育过程中,B细胞可能发生恶性转化,导致白血病或淋巴瘤。这种转化通常是由基因事件引发的,导致异常表达的蛋白质,促进细胞的生长和生存。然而,突变通常不足以导致癌症的发展。相反,恶性B细胞的生存和扩张严重依赖于与其微环境细胞的相互作用[6-8]。
B细胞恶性肿瘤常由GC B细胞引起。因此,GC内的细胞在白血病和淋巴瘤的发病、进展和复发过程中是恶性细胞的关键合作伙伴。除非造血细胞如间充质间质细胞和成纤维细胞外,GC还含有Tfh细胞,Tfh细胞支持B细胞的生理成熟和功能。有趣的是,恶性转化的B细胞似乎保留了与Th细胞相互作用的能力,因此仍然能够从Th细胞的帮助中获利。因此,对适应性免疫应答至关重要的Th细胞介导的支持——当指向恶性B细胞时——可以促进淋巴瘤或白血病(图1)。

图1:恶性Th细胞- b细胞相互作用的机制
滤泡性淋巴瘤(FL)是一种由GC B细胞引起的惰性淋巴瘤。非造血细胞和Th细胞在支持FL细胞生长和存活[9]中都起着关键作用。来自FL感染淋巴结的Tfh细胞表达升高的IL-2、IL-4、IFN-γ和TNF -[10]水平,似乎通过IL-4支持FL细胞[11,12]。除细胞因子外,CD40与CD40L的连接也起作用。当CD40交联刺激FL细胞时,细胞存活率增加在体外提示CD40L刺激可通过NF-κ b依赖的方式保护FL细胞免受trail介导的凋亡。
伯基特淋巴瘤(Burkitt’s lymphoma, BL)是一种侵袭性B细胞癌,可能起源于GC B细胞[16]BL与eb病毒(EpsteinBarr virus, EBV)密切相关,尽管其发病机制尚不清楚[17,18]。Th细胞在BL发育和进展中的作用一直存在争议。多项研究表明,eb病毒特异性Th细胞可以杀死或限制BL细胞系或eb病毒转化的B细胞的增殖[19-27]。相反,也有报道称,eb病毒特异性Th细胞可以诱导B细胞增殖[28],在一些小鼠模型中,这种eb病毒特异性Th细胞甚至在淋巴瘤发生中是必需的[29-31]。两项研究发现Th细胞既具有杀伤作用,又具有支持作用[32,33],提示Th细胞在BL和其他ebv相关恶性肿瘤中的功能可能与环境相关。
在霍奇金淋巴瘤(Hodgkin lymphoma, HL)中,某些Th细胞亚群的浸润与患者总生存期的降低相关[34,35]。几种细胞因子似乎对HL的恶性细胞有刺激作用,其中之一是Th2细胞因子IL-13[36]。然而,这种细胞因子的来源仍不清楚。因此,Th细胞在HL发育或扩张中的直接作用仍有待证实。
慢性淋巴细胞白血病(CLL)是一种成熟克隆B细胞的恶性肿瘤,尽管确切的细胞来源仍有争议[37]。CLL细胞在次级淋巴器官的假滤泡中增殖,并在骨髓中接受基质微环境[38]细胞的支持。Th细胞通过趋化因子被CLL细胞积极招募,浸润这种CLL假滤泡[39,40]。最近,我们发现这些Th细胞识别来自自体CLL细胞的抗原,并以抗原和cd40l依赖的方式刺激CLL细胞的激活和增殖在体外在一个在活的有机体内异种移植模型[41]。有趣的是,患者来源的cll特异性Th细胞具有Th1样表型,特征是高IFN-γ分泌。IFN-γ上调CD38,这是CLL中预后不良的标志,其机制涉及IFN-γ诱导转录因子T-bet结合到CD38基因5个调控区域的两个共识位点[42,43]。一致地,外周血CLL细胞中T-bet表达与CD38表达显著相关。因此,似乎Th细胞通过分泌IFN-γ促进更具侵略性的CLL亚群的发展。
CLL细胞表达多反应性和/或自反应性BCR,提供一定水平的恒定信号[44,45]。然而,持续的BCR信号通路可诱导能量缺失和细胞凋亡。事实上,CLL细胞被认为是自反应的B细胞,可以通过微环境的刺激从无能量状态中拯救出来[46,47]。一致地,我们发现CD40L的刺激激活了CLL细胞中的激酶Syk,这是BCR和CD40信号级联共有的一个成分。这表明Th细胞通过CD40L刺激[48]将CLL细胞从无能量状态中拯救出来,从而促进了CLL的发展。
多发性骨髓瘤(MM)是一种恶性肿瘤,其特征是浆细胞源性骨髓瘤细胞在骨髓内的扩张。MM患者BM表现为T细胞[49]增多,CD40刺激诱导MM细胞迁移,与MM疾病进展[50]相关。CD40刺激还可触发MM细胞分泌IL-6, IL-6可能通过自分泌和/或旁分泌机制介导MM细胞增殖[51]。除了cd40l介导的刺激外,MM-特异性Th细胞还可以通过分泌细胞因子[52]支持自体MM细胞。最近,我们证实了多克隆激活的异体和自体Th细胞以cd40l依赖的方式刺激MM细胞的成胚和增殖。结合前人的报道,提示CD40L刺激是Th细胞介导的MM细胞支持的关键机制,但IL-6、IL-17等细胞因子也是重要的组成部分。
肿瘤微环境在支持恶性细胞方面起着关键作用。在B细胞白血病和淋巴瘤中,恶性B细胞似乎保留了从其生理相互作用伙伴Th细胞获得帮助的能力。一直以来,Th细胞在各种类型的B细胞恶性肿瘤中的癌症支持作用已被描述,尽管具体机制仍有待确定。有效的抗癌治疗应该包括靶向肿瘤微环境的细胞。因此,识别和表征促肿瘤Th细胞和恶性B细胞之间的协同作用的研究工作可能为针对肿瘤微环境的治疗提供新的策略。
在此处下载临时PDF
文章类型:评论文章
引用:burkers S (2017) B细胞和T辅助细胞之间的恶性相互作用。J Blood Disord Med 2(1): doi http://dx.doi.org/10.16966/2471-5026.115
版权:©2017 burer s。这是一篇开放获取的文章,在知识共享署名许可的条件下发布,该许可允许在任何媒体上无限制地使用、传播和复制,前提是原始作者和来源被注明。
出版历史:
所有Sc德赢娱乐国际i Forschen期刊都是开放获取的